

多硫化锂外溶剂壳中的溶解能力对EPSE封装的重要性
电子说
描述
全文概要
长循环寿命是锂硫电池实际应用的先决条件,但受到可溶性多硫化物与锂金属负极之间的副反应的限制。对多硫化物溶剂化结构的调节使封装多硫化物电解质(EPSE)成为抑制副反应的有前景的解决方案。多硫化锂外溶剂壳中溶剂的溶解能力对于EPSE的封装效果至关重要。
在这里,来自清华大学的张强、北京理工大学张学强团队证明了一种典型的氢氟醚1, 1, 2, 2-四氟乙基-2, 2, 3, 3-四氟丙基醚(HFE)是构建EPSE的优良外壳溶剂。基于氟烃链的大空间位阻,吸电子-CF2-链段进一步赋予HFE分子显著弱的溶剂化能力。HFE-EPSE将具有超薄锂金属负极(50 μm)和高面载量硫正极(4.4 mg cm-2)的锂硫电池的寿命从54次循环提高到135次。
此外,具有HFE-EPSE的334 Wh kg-1锂硫软包电池(2.4 Ah水平)可稳定循环25次。这项工作证明了削弱多硫化锂外壳溶剂的溶剂化能力对构建优质EPSE的重要作用,并启发了调节多硫化物的溶剂化化学以实现锂硫电池长循环寿命的意义。

文章亮点
1、提出了一种全新的封装多硫化物电解质(EPSE)概念,以抑制LiPS在锂金属负极上的副反应,同时保持较好的硫氧化还原反应转化动力学。
2、在这项工作中,1, 1, 2, 2-四氟乙基-2, 2, 3, 3-四氟丙基醚(HFE)被证明是构建EPSE以抑制LiPS在工作锂金属上的副反应的优良外壳溶剂负极,显著提高了Li-S电池的循环性能。
正文导读
氟烃链的大空间位阻和HFE分子中的吸电子-CF2-链段都确保了显著弱的溶剂化能力。HFE仅分布在LiPS周围的外溶剂壳中,几乎不改变LiPS的内溶剂壳。HFE-EPSE使用50 μm的超薄锂金属负极和4.4 mg cm-2的高面载量S正极,将Li-S电池的循环寿命从54次循环提高到135次。此外,具有HFE-EPSE的2.4 Ah软包电池可稳定循环25次,初始能量密度为334 Wh kg-1。
(1)HFE-EPSE的溶剂化结构
大的空间位阻使分子具有弱的溶剂化能力,可以用作LiPS的外壳溶剂来构建EPSE。氢氟醚不仅对氟烃链有较大的空间位阻,而且还有丰富的吸电子C-F链段(如-CF2-和-CF3)。与DIPS和DIPE相比,C-F键的吸电子效应赋予氢氟醚极低的溶剂化能力。因此,预计氢氟醚具有调节LiPS溶剂化结构的潜力,特别是作为LiPS外壳溶剂的有希望的候选化合物。
本文选择1, 1, 2, 2-四氟乙基-2, 2, 3, 3-四氟丙基醚(表示为HFE)作为代表性氢氟醚,以展示构建EPSE的潜力。HFE-EPSE由1,3-二氧戊环(DOL)/1,2-二甲氧基乙烷(DME)/HFE(体积比2:2:1)组成。DOL/DME(体积比1:1)由于其自2000年代以来在锂硫电池中的广泛应用而被用作典型的对照溶剂。
两种电解质均含有1.0 M双(三氟甲磺酰基)酰亚胺(LiTFSI),以提供基本的离子电导率。 通过分子动力学(MD)模拟解码了1.0 M [S] Li2S8的溶剂化结构,即DOL/DME或HFE-EPSE中LiPS周围的溶剂分布。在DOL/DME和HFE-EPSE中,Li+与S82−紧密相互作用,这意味着Li2S8的解离很弱(图1a、1d)。
在DOL/DME中,DME从S82−中心通过S82−-Li+-溶剂相互作用在4.4 Å处出现,并形成内溶剂壳(壳1)。在DME之后,DOL出现在6.6 Å处,形成外溶剂壳(壳2)。1.0 M [S] Li2S8的溶剂化结构与之前的研究相似。Li+、DME和DOL的配位数分别从2.1、4.0和4.8 Å开始增加,这也反映了LiPS周围溶剂溶解能力的差异(图1b、1c)。
将HFE引入DOL/DME极大地改变了LiPS外溶剂壳,而不是内溶剂壳。具体来说,LiPS周围的内溶剂壳由DME(4.4 Å)组成,这与DOL/DME中的类似,以确保LiPS的适当溶解。HFE出现在6.4 Å,它在第二个溶剂壳中被捕获(图1d)。Li+、DME、DOL、HFE在中心S82−周围的配位数分别在2.1、4.0、4.8和5.5 Å处开始增加,表明HFE仅影响外溶剂壳的结构,但封装了中心S82−和内溶剂壳(图1e、1f)。
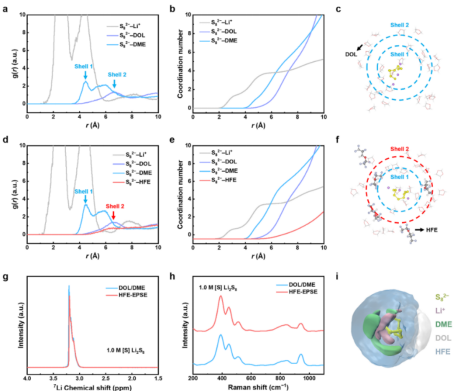
【图1】LiPS溶剂化结构。(a)径向分布函数(g(r)),(b)配位数,和(c)DOL/DME中S82-周围的分子分布快照。(d)径向分布函数(g(r)),(e)配位数,和(f)HFE-EPSE中S82-周围的分子分布快照。径向距离(r)是从选定S82-的质心到其他组成的距离。H、Li、C、O、F和S原子分别用白色、紫色、灰色、红色、浅紫色和黄色球表示。DOL分子以线框形式显示,而DME和阴离子分子为清楚起见未显示。(g)1.0 M [S] Li2S8在HFE-EPSE和DOL/DME中的7Li-NMR谱和(h)拉曼光谱。(i)HFE-EPSE的空间分布函数(SDF)。DME、DOL、Li+和HFE的空间分布函数的等值分别为5.5、4.0、20.0和0.4。
进一步采用包括核磁共振(NMR)和拉曼光谱在内的实验来探测LiPS的溶剂化结构。考虑到溶剂通过S82−-Li+-溶剂相互作用与LiPS相互作用,7Li-NMR被用来推断溶剂在LiPS周围的分布。选择溶解在DOL/DME或HFE-EPSE中的1.0 M [S] Li2S8作为电解质,以模仿MD模拟中使用的电解质配方。
对于DOL/DME和HFE-EPSE,7Li的化学位移均为3.20 ppm,表明HFE几乎不与Li+相互作用,并且不会改变LiPS的内溶剂壳(图1g)。与以往研究认为DIPS和DIPE的引入对7Li化学位移的去屏蔽效应影响不大,HFE-EPSE的解码溶剂化结构表明,HFE的溶剂化能力远弱于DIPS和DIPE,这得益于氟烃链的大空间位阻和-CF2-链段的吸电子作用。拉曼光谱也有类似的结论。
多硫化物(392、448和510 cm-1)、DME(845 cm-1)和DOL(945 cm-1)的信号几乎与DOL/DME和HFE-EPSE重叠,表明内溶剂LiPS周围的外壳随着HFE的引入而保持(图1h)。1.0 M [S] Li2S6也得到了类似的结论。因此,可以得出结论,HFE成功构建了EPSE(图1i)。
在以往的研究中,针对锂离子和锂金属电池提出了局部高浓度电解液的概念,氢氟醚的引入旨在降低锂盐的表观浓度,但使电解液呈现高浓度的溶剂化结构电解质。氢氟醚由于溶剂化能力差,不参与锂离子的溶剂化。几乎所有具有强溶剂化能力的溶剂都参与了Li+的溶剂化结构,甚至阴离子直接与Li+相互作用形成接触离子对(CIP)和聚集体(AGG)。
因此,当这种策略转移到Li-S电池时,由于配位溶剂供应不足,LiPS在局部高浓度电解质中的溶解度被限制在<100 mM [S] ,并且很少关注LiPS溶剂化结构。相比之下,HFE-EPSE中仍有丰富的具有强溶剂化能力的游离溶剂,因此可以保持LiPS的溶解度和正极的正常转化。HFE仅分布在外溶剂壳中,这有望减少LiPS与锂金属负极的接触。
(2)HFE-EPSE抑制LiPS的副反应
通过电化学测试研究了HFE的还原稳定性。在循环伏安(CV)测试期间,还原电流分别在DME和DOL的1.2和0.9 V处开始增加(图2a)。DME和DOL的相应峰值电流分别为0.054和0.024 mA cm-2。相比之下,HFE的还原电流仅为0.01 mA cm-2,表明HFE具有出色的还原稳定性。
在没有LiNO3添加剂的情况下,研究了HFE-EPSE在温和条件下抑制副反应的效果,LiNO3添加剂是稳定锂硫电池中锂金属负极的最有效添加剂之一。具有HFE-EPSE和DOL/DME的Li-S电池的初始放电容量相似(1001对969 mAh g-1)(图2b)。具有两种电解质的Li-S电池的恒电流放电-充电曲线几乎重叠(图2c),表明LiPS在正极的转化动力学较好。
使用HFE-EPSE电解质的Li-S电池在15次循环后的容量保持率比使用DOL/DME的62%更高(图2b)。使用HFE-EPSE可提高库仑效率(CE)。在第二个循环中,使用HFE-EPSE电解质的Li-S电池的CE比使用DOL/DME的电池的56.2%更高,为70.4%(图2c)。
增加的CE表明HFE-EPSE显著减少了LiPS的穿梭。此外,在2.2至2.6 V的不同恒电位测试中,HFE-EPSE可将穿梭电流降低约60 mV(图2d)。因此,常规电解质中的DOL和DME不能封装中心的LiPS,从而导致LiPS在锂金属负极上发生严重的副反应(图2e)。相比之下,HFE-EPSE可以有效地封装居中的LiPS并减少LiPS的副反应(图2f)。
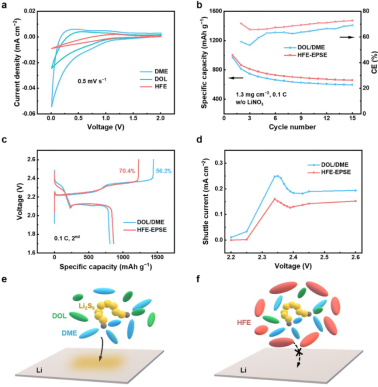
【图2】不含LiNO3的Li-S电池的电化学性能。(a)DOL、DME和HFE的还原稳定性测试。(b)循环性能,(c)恒电流放电-充电曲线,和(d)穿梭电流。(e)LiPS与锂负极在DOL/DME电解液中的严重副反应和(f)HFE-EPSE中抑制的副反应的示意图。
(3)实际条件下的HFE-EPSE锂硫电池
锂硫电池的测试条件对策略的评估客观性有很大影响。尽管锂硫电池可以在常规负载S正极小于2 mg cm-2和足够的锂供应(厚度超过500 μm)的常规条件下提供较长的使用寿命,但温和的条件掩盖了锂金属负极的问题并且夸大了负极保护策略的有效性,因为在每个循环中仅使用了低比例的锂金属负极(<4%)。
因此,HFE-EPSE在高负载硫正极(4.4 mg cm-2)、超薄锂负极(50 μm)和硫电解液(E/S)等苛刻条件下在锂硫电池中的实际效果得到验证。6.0 μL mgS-1与LiNO3添加剂的比例(图3a)。在0.05 C的初始两个激活循环后,Li-S电池在0.1 C循环。
具有DOL/DME电解质的Li-S电池的初始比容量为957 mAh g-1(图3a)。然而,比容量在40次循环后急剧下降。基于70%的容量保持率,具有DOL/DME的Li-S电池仅提供54个循环。相比之下,基于70%的容量保持率,具有HFE-EPSE的电池经历了稳定的135次循环。
使用HFE-EPSE后,Li-S电池的循环寿命提高了1.5倍。与其他先进的电解质策略相比,采用HFE-EPSE的电池的循环稳定性更好。使用HFE-EPSE的电池的放电中值电压即使在135次循环后仍保持稳定在2.06 V以上,而使用DOL/DME的电池在20次循环后急剧下降,在40次循环后仅达到2.00 V(图3b)。
HFE-EPSE实现的更稳定和更高的放电中值电压表明电池的内阻降低,死锂积累得到缓解。具体来说,除了放电容量略有差异外,具有DOL/DME和HFE-EPSE的Li-S电池在第2次循环时的恒电流充电和放电曲线几乎重叠(图3c)。此外,使用HFE-EPSE的Li-S电池的放电曲线在第40次循环时保持稳定,而使用DOL/DME的锂硫电池在第二次放电平台时提供了显著的斜率。
DOL/DME增加的极化表明活性锂储层不足,这不仅导致寿命短,而且降低了能量密度。此外,研究了HFE-EPSE的倍率性能。具有HFE-EPSE的Li-S电池在0.1、0.2、0.3、0.4和0.5 C下的比容量分别为957、885、837、778和738 mAh g-1,表明HFE-EPSE可以以不同的倍率有效工作。
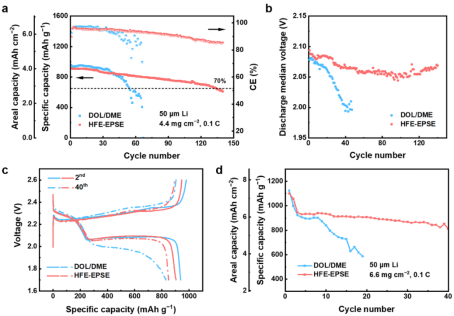
【图3】LiNO3锂硫电池的电化学性能。(a)具有DOL/DME和HFE-EPSE电解质的全电池在苛刻条件下的循环性能。(b)放电中值电压和(c)Li-S电池的恒电流放电-充电曲线。(d)具有6.6 mg cm-2的高负载S正极和6.9 μL mgS-1的E/S比的全电池的循环性能。
采用6.6 mg cm-2的高负载S正极来证明HFE-EPSE的效果。相应的实际N/P比为1.4,远低于S正极为4.4 mg cm-2的Li-S电池的2.6。较低的N/P比对应于较高的锂利用率(71% vs. 38%)和较高的锂利用率(7.4 vs. 3.9 mAh cm-2),这表明副反应更严重,可以验证HFE-EPSE的影响。
在具有HFE-EPSE电解质的Li-S电池中,初始比容量为1100 mAh g-1,在0.1C下循环40次后容量保持率为74%(图3d)。相比之下,在具有DOL/DME电解质的Li-S电池中观察到初始比容量为1123 mAh g-1,但在19次循环后容量保持率低至52%。具有HFE-EPSE的Li-S电池在循环过程中也表现出低放电电压极化。HFE-EPSE有效地延长了锂硫电池在苛刻条件下的循环寿命。
分析循环的锂金属负极,以验证HFE-EPSE在抑制副反应方面的优势。具有DOL/DME的Li-S电池中的残余锂在40次循环后暴露于Cu集流体时是随机分布且不均匀的,而在HFE-EPSE中残余锂更紧凑。通过基于循环锂的剥离测试分析了锂硫电池中锂金属负极在40次循环后的剩余活性锂储层。镍电池配置。
具有HFE-EPSE的Li-S电池的剩余活性锂储层为7.3 mAh cm-2,占原始活性锂的73%(图4a)。具有DOL/DME的Li-S电池的剩余活性锂储层为6.1 mAh cm-2,低于HFE-EPSE。通过X射线光电子能谱(XPS)分析锂金属负极上的S原子含量,以评估LiPS的副反应程度。
与DOL/DME电解液相比,HFE-EPSE中锂金属负极的S含量在120秒溅射过程中有所降低(在0、30、60、90和120s溅射时分别为4.87% vs. 5.61%、5.16% vs. 5.84%、4.87% vs. 6.14%、5.04% vs. 5.95%,以及5.10% vs. 5.81%),表明HFE-EPSE抑制了LiPS的副反应(图4b)。
SEI中的含氟(LiF和C-F)和含氮(LiNxOy)物质在两种电解质中是相似的。采用HFE-EPSE的锂硫电池的阻抗为15.3欧姆,小于采用DOL/DME的锂硫电池的20.2欧姆(图4c)。HFE-EPSE实现的低阻抗表明,HFE-EPSE减轻了死锂的积累。通过扫描电子显微镜观察进一步研究了锂的沉积行为。
在DOL/DME中循环的锂沉积是不均匀的,具有随机裂纹和锂枝晶,这意味着LiPS与工作中的锂金属负极会发生严重的副反应(图4d)。相比之下,使用HFE-EPSE的锂沉积是均匀且紧凑的(图4e)。在工作的Li-S电池中,HFE-EPSE抑制了LiPS与锂金属负极的副反应。
此外,Li|Cu和Li|Li电池用于评估Li剥离/沉积的均匀性。Li|具有HFE-EPSE的Cu电池在1.0 mA cm-2和1.0 mAh cm-2的60次循环中平均CE为94.2%,高于DOL/DME的87.4%。Li|与在1.0 mA cm-2和1.0 mAh cm-2下的DOL/DME(13 vs. 61mV,120小时)相比,具有HFE-EPSE的Li电池在120小时内表现出较低的电压极化。使用HFE-EPSE提高了Li剥离/沉积的均匀性。
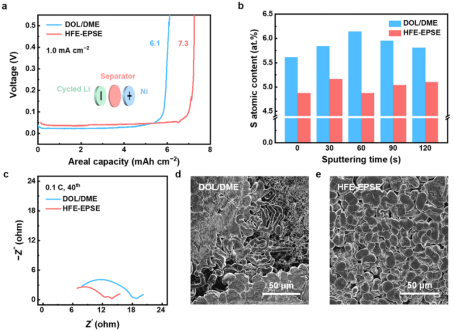
【图4】第40次循环Li硫电池的分析。(a)Li剥离试验的残余Li储层。(b)XPS在不同溅射时间期间探测到的负极上的S含量。(c)循环Li硫电池的电化学阻抗谱。(d)常规DOL/DME和(e)HFE-EPSE电解液中Li沉积物的形态。
(4)具有HFE-EPSE的实用Li-S软包电池
与扣式电池相比,软包电池可以从器件规模上展示出Li硫电池的高能量密度优势,并为验证策略的有效性提供了非常苛刻的条件。采用2.4 Ah级软包电池来验证HFE-EPSE的效果(图5a)。电极中的活性材料为双层,电极尺寸为7·4 cm2。采用高负载S正极(7.2 mg cm-2)、超薄Li金属负极(75 μm)和贫电解质(3.5 g gS-1)构建全电池。初始放电能量密度为334 Wh kg-1(图5b)。
经过25次循环后,具有HFE-EPSE的软包电池具有60%的高容量保持率和相对稳定的CE(图5c)。Li-S电池在循环过程中表现出典型的两个放电平台,表明在HFE-EPSE电解液中保持了固-液-固硫氧化还原反应(图5d)。HFE-EPSE有望与正极氧化还原促进剂(如电化学催化)具有良好的相容性,以改善转化动力学。因此,HFE-EPSE成为一种有前景的实用长循环和高能量密度Li-S电池的解决方案。
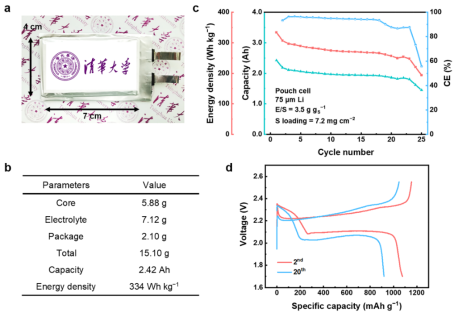
【图5】Li-S软包电池的循环性能。(a)光学图像和(b)软包电池的参数。核心包括Li负极、硫正极、Cu集流体、铝集流体、隔膜和极耳。(c)Li-S软包电池的循环性能和(d)相应的恒电流放电-充电曲线。
总结与展望
HFE被用作构建EPSE的优良外壳溶剂,以抑制LiPS和Li金属负极之间的本征副反应。HFE分子中有两条空间位阻大的长碳氟烃链和丰富的吸电子-CF2-链段,这使得HFE的溶剂化能力非常弱。HFE与LiPS的弱相互作用使得HFE仅分布在LiPS的外溶剂壳中。
具有高还原稳定性的HFE可确保在重复循环过程中很好地保存封装结构。HFE-EPSE在超薄Li金属负极(50 μm)和高负载硫正极(4.4 mg cm-2)的容量保持率达到70%的基础上,将Li-S电池的循环寿命从54次循环提高到135次。此外,具有HFE-EPSE的2.4 Ah级Li-S软包电池可提供稳定的25次循环,初始能量密度为334 Wh kg-1。这项工作表明,HFE是构建EPSE的优良外壳溶剂,并激发了对LiPS溶剂化结构的进一步有效调控,以实现长循环Li-S电池。
审核编辑:刘清
-
求助,ADC接地的重要性?2024-06-04 0
-
硫化氢检测仪中应用的硫化氢传感器2018-08-10 0
-
基准源设计的重要性2019-06-18 0
-
代码规范的重要性是什么2020-05-19 0
-
绝缘测试的重要性2020-12-23 0
-
时钟的重要性2021-08-13 0
-
时钟系统的重要性2021-08-20 0
-
论调节阀的重要性2021-09-15 0
-
时钟服务器的重要性是什么?2021-11-08 0
-
UPS的重要性2021-11-16 0
-
arm汇编的重要性是什么?2021-11-30 0
-
POE浪涌保护的重要性是什么?2022-01-14 0
-
高能效新的纳米硫化锂/硅电池2010-03-02 798
-
半导体封装在半导体产业链中的重要性2020-10-21 2847
全部0条评论

快来发表一下你的评论吧 !

