

浅析在锂离子电池中使用LiFSI作为单一电解质溶液的适用性
电池技术
描述
一、全文概要
来自美国陆军研究实验室的张升水通过研究在3:7(重量)碳酸亚乙酯/碳酸甲乙酯电解液中研究铝和不锈钢(SS)的腐蚀行为,揭开双(氟磺酰基)亚胺锂(LiFSI)作为单盐在锂金属和锂离子电池的中低浓度电解液中的适用性之谜。研究发现,无论LiFSI浓度如何(0.8-1.8 m),“阈值电位”与Li/Li+的关系为~4.3 V,高于该阈值时,Al会遭受无法控制的腐蚀。
这一发现在石墨/LiNi0.80Co0.15Al0.05O2软包电池中得到证实,但是,在第一次充电时,没有一个Li/LiNi0.80Co0.10Mn0.10O2扣式电池可以充电至4.2 V。对失效扣式电池的分析表明,失效是由于SS垫片的负极腐蚀造成的。对SS304和SS316L两种垫片的进一步研究表明,SS316L垫片更耐腐蚀,但仍不能支持电池的长寿命循环。
只要在正极处将充电电压严格限制在“阈值电位”并避免使用SS成分,就可以保证在锂离子电池中使用LiFSI作为单一电解质溶液的适用性。通过使用四种不同来源的LiFSI进一步验证了这一结论。
二、正文部分
1、文章亮点
1、在这项工作中,使用碳酸亚乙酯和碳酸甲乙酯的3:7(wt)溶剂体系研究了LiFSI浓度对Al集流体和不锈钢(SS)垫片负极腐蚀的影响。
2、这项工作有两个重要的发现:(1)无论LiFSI浓度如何,都有一个~4.3 V vs. “阈值电位”的Li/Li+,高于该电位时,Al会遭受无法控制的腐蚀,以及(2)扣式电池的失效仅仅是由于SS垫片的腐蚀。
3、只要在正极处将充电电压严格限制在“阈值电位”并且避免使用SS组件,就可在锂金属和锂离子电池的中低浓度电解质中使用LiFSI作为单盐。通过使用四种LiFSI来源进一步验证了这种适用性。
2、正文导读
Al的腐蚀行为——使用浸入式三电极电池,通过循环伏安法在0.1 mV s-1的缓慢速率下研究Al在各种LiFSI浓度电解液中的腐蚀行为。
最初三个循环如图1所示,从中可以观察到几个重要发现:首先,无论LiFSI浓度如何,在铝表面上形成的天然氧化铝钝化层都能够保护铝免受负极腐蚀。如图1a至图1e中第一个循环的负极电流所示,到4.3 V vs. Li/Li+,在此之上,Al会遭受无法控制的腐蚀。
可以观察到,在第一个循环中,即使电位从最大值(5.5 V)向下扫描,负极电流也会继续增加。这种行为只有在腐蚀失控时才会发生,因为在这种情况下,电流与未保护的铝的表面积成正比,后者在不可控的过程中随着原生氧化铝钝化层的击穿时间而增加腐蚀成都。其他文章也报道了类似的腐蚀模式,并且发现此类腐蚀是由溶剂氧化引起的,这不仅受溶剂性质的影响,还受盐浓度和溶剂组成的影响。
换句话说,这种腐蚀的起始电位受电解质溶剂氧化的影响,而不是受铝的性质影响。为了区分,这种起始电位被称为“阈值电位”。
因此,之前关于LiFSI电解质中铝腐蚀的许多争议可以通过电解质溶剂对“阈值电位”的影响来合理解释。这也部分解释了HCE策略的成功,因为高盐浓度降低了溶液中游离溶剂的摩尔分数,从而提高了溶剂在极端电位下抗氧化和还原的稳定性。
其次,与第一个循环相比,在所有LiFSI浓度下,第2和第3循环的起始电位持续下降0.2-0.3 V。这是因为Li参比电极与从工作电极上溶解的Al3+离子发生反应,形成Li-Al合金,从而提高了Li参比电极的标准电极电位。第三,在实验结束时(6个循环),Al工作电极和Li参比电极的表面颜色分别变为黑色和灰色,最显著的是,在Li对电极周围聚集了大量灰色絮状物(见每个图中的图片,其中锂对电极用符号“c”标记)。
上图中,黑色Al表面意味着Al腐蚀伴随溶剂氧化,灰色Li参比电极表明Li表面形成了Li-Al合金,而灰色絮状物,其数量随着腐蚀的减少而急剧增加。LiFSI浓度是锂金属、锂铝合金和溶剂分解产物的混合物。另一方面,图1f表明,对于0.8 m至1.2 m LiFSI的低浓度,在3.5 V vs. Li/Li+附近偶尔会发生轻微腐蚀。
然而,这些轻微的腐蚀是自我修复的,如负极电流的小峰值所示(参见图1f中标记的点矩形)。从上述结果可以得出结论,只要充电电压严格限制在正极。
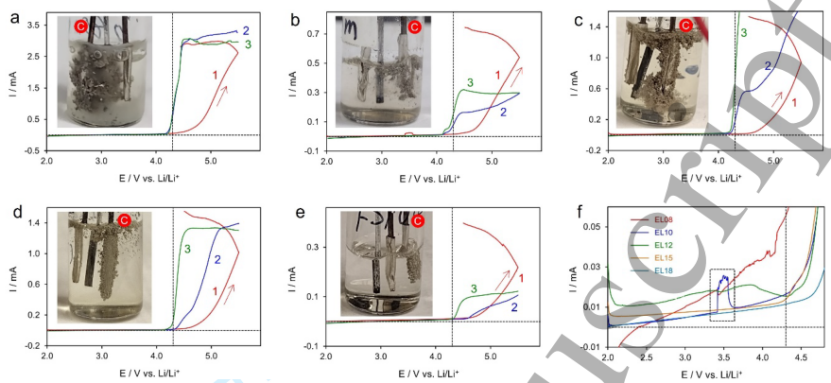
【图1】Al-Li-Li三电极电池的初始三个循环伏安图的部分,其中插图显示了电池在0.1 mV s-1与Li/Li+之间在2.0 V和5.5 V之间连续六个循环后的照片。(a)EL08,(b)EL10,(c)EL12,(d)EL15,(e)EL18,(f)第一次电位扫描中负极电流的比较。
锂离子软包电池的成功——根据上述发现,在200 mAh Gr/NCA软包电池中研究了LiSFI电解质。图2比较了使用不同LiFSI浓度电解质的软包电池的第一次循环电压曲线和放电容量。
特别是,前两个循环的容量和库伦效率总结在表1中。从图2和表1中可以看出,由LiFSI浓度引起的循环性能差异在误差范围内。在第2个循环中,所有电池的容量都有小幅增加(参见图2b和表1)。特别是具有0.8 m LiFSI电解质的电池在第22次循环中容量损失很小。
这归因于轻微的铝腐蚀,并在随后的循环中自我修复,如图1f所示。考虑到成本和电池性能,1.2-1.5 m的浓度范围似乎是锂金属和锂离子电池中使用的LiFSI电解质的最佳选择。此外,如图2b所示,由于测试室的昼夜温度变化,可以发现容量的小而有规律的波动。
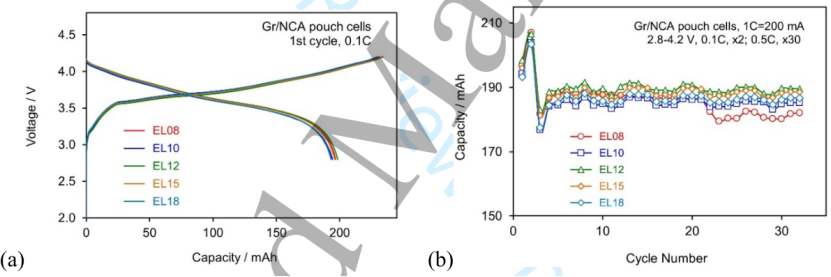
【图2】Gr/NCA软包电池的循环性能。(a)0.1 C下第一个循环的电压曲线,和(b)0.5 C下循环的电池的放电容量,但最初的两个循环在0.1 C下除外。
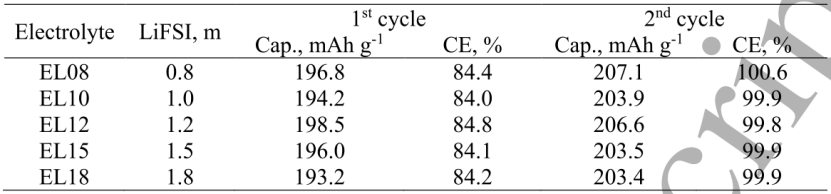
【表1】LiFSI浓度对Gr/NCA软包电池比容量和库仑效率的影响
扣式电池失效——在Li/NCM811扣式电池中测试了相同的电解质,但是没有一个电池可以充电到截止电压(4.2 V)。图3显示了Li/NCM811扣式电池第一次充电的电压曲线,通过将电池在0.1 C(1 C=1.68 mA cm-2)下将电池充电至4.2 V,然后在4.2 V下保持一段时间来记录。
总共100小时。结果表明,在达到4.2 V之前,所有电池的电压都开始通过两个平台模式下降。对测试电池的事后分析表明,所有失效都是由于SS垫片(由SS304制造)的腐蚀造成的,并且电池电压下降的模式对应于以下两个过程:(1)过渡的氧化还原穿梭Fe2+/3+、Ni2+/3+和Cr2+/3+等离子被SS垫片的负极腐蚀溶解,用于第一个较高的电压平台,以及(2)局部电短路,由沉积的金属枝晶,用于第二个较低的电压平台。
图4a和图4b分别显示了电池组件的图片和SS垫片的腐蚀图像。非常一致地观察到,锂负极的外边缘完全被许多黑色沉积物覆盖,SS垫片被严重腐蚀。
特别是,Al集流体变得非常脆弱,并在与水接触时立即产生气泡,这为局部电短路提供了极好的支持。正是局部电短路促进了铝集流体通过原电池与锂负极反应,而铝集流体和锂负极之间不需要物理接触,形成锂铝合金并使铝箔非常易碎。
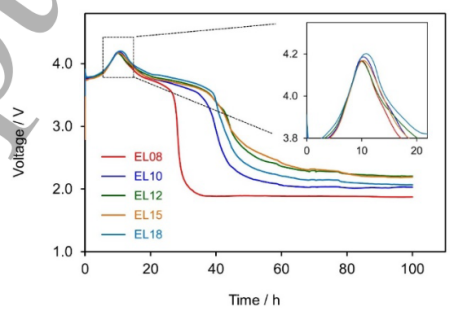
【图3】使用SS304垫片的Li/NCM811扣式电池首次充电的电压曲线,通过将电池设置为0.1 C充电至4.2 V并在4.2 V下保持总共100小时。
从图4a中的所有SS垫片观察到环形腐蚀图案。使用水清洗垫片并显示在图4b中,从中发现腐蚀环的尺寸和形状与正极的尺寸和形状完全匹配。
这是因为一方面离子传输路径被固态铝集流体阻挡,从而保护正极下方的SS垫片免受负极腐蚀,另一方面,多余的液态电解质优先沿较小正极的外边缘积聚,这使得这些区域的极化程度较低,因此比其他区域更容易腐蚀。

【图4】(a)扣式电池组件的照片,在Li/NCM811电池在0.1 C下充电100小时后收获,和(b)显示正极形状和尺寸腐蚀环的代表性垫片和腐蚀的显微镜图像,随机选自不同浓度的电解质。
SS304与SS316L垫片——有两种类型的扣式电池垫片,由SS304和SS316L制造。表2比较了SS304和SS316L的化学成分和耐腐蚀性,图5显示了采用1.2 m LiFSI电解质的Gr/NCM811扣式电池的性能。如图5a所示,在第一次充电中,使用SS304垫片的电池未能达到4.2 V,而另一个使用SS316L垫片的电池在2.8 V和4.2 V之间完成了第一次充放电,表明SS316L垫片的耐腐蚀性优于SS304垫片。
因此,分别使用4.1 V和4.2 V的截止电压选择SS316电池进行进一步的循环测试,结果如图5b所示。结果表明,截止电压为4.2 V的电池的比容量和库仑效率均显著低于截止电压为4.1 V的电池。即使在4.1 V下截止,电池的容量仍会随着循环而迅速衰减数字。
上述结果表明,LiFSI电解质与不锈钢材料在电化学上不相容,这可能是使用扣式电池进行测试的不同研究人员报告的结果不一致的部分原因。
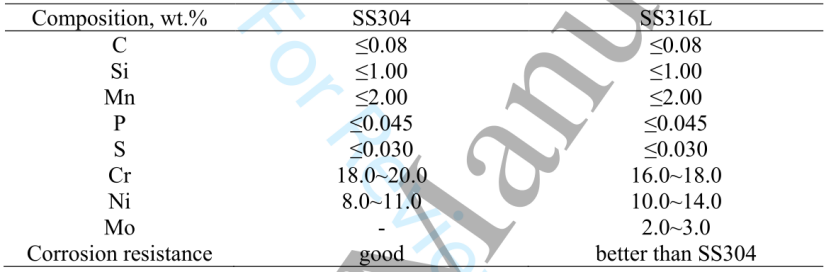
【表2】SS304和SS316L的化学成分和耐腐蚀性
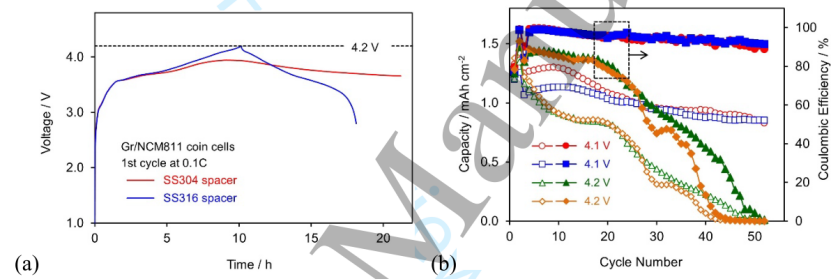
【图5】Gr/NCM811扣式电池的性能差异是由垫片的SS材料引起的。(a)第一个循环在0.1 C时的电压曲线,和(b)放电容量(空心符号)和库仑效率(实心符号),每个截止电压有两个电池。
图6显示了使用SS304垫片测试的Gr/NCM811电池的图片和腐蚀图像。再次,从垫片观察到环形腐蚀图案,并且在面向Gr负极和Gr负极的一侧的垫片的外边缘完全被黑色沉积物覆盖,据报道这些黑色沉积物是电解质的分解产物溶剂。大量黑色分解产物表明溶剂分解一定是由从SS间隔物中溶解的过渡金属离子(Fe、Ni和Cr)的还原催化的。

【图6】Gr/NCM811扣式电池中SS304垫片在0.1 C充电100小时后的腐蚀行为。(a)SS垫片,(b)面向Gr负极一侧的垫片,和(c)Gr负极。
LiFSI的不同来源——基于上述分析,认为在锂金属和锂离子电池的中低浓度电解质中使用LiFSI作为单盐是合适的,只要在正极处,充电电压严格限制在“阈值电位”,并且避免使用SS组件(目前工作中为4.2-4.3 V vs. Li/Li+)。为了验证这一假设,使用四种LiFSI来源制备1.2 m的电解质,分别编码为EL12[A]、EL12[B]、EL12[C]、EL12[D],并在Gr/NCA软包电池中进行研究.这些电池的循环性能在图7中进行了比较,在0.1 C下最初两个循环的数据总结在表3中。与图2和表1中观察到的相似,与LiFSI来源相关的差异在误差范围。
再次观察到从第一个循环到第二个循环的容量小幅增加。由于在所有电池中始终观察到如此小的容量增益,因此可以认为这是软包电池的普遍现象,可以通过第一次充电和放电消除电极和隔膜之间的机械应力来解释,从而使电解质均匀化分布并降低电池的内阻。
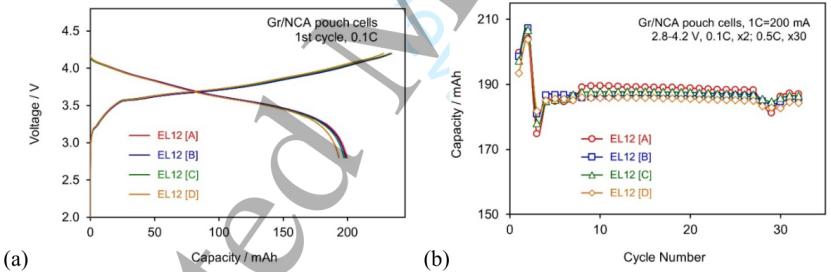
【图7】使用不同来源的LiFSI制成的1.2 m LiFSI电解质的Gr/NCA软包电池的循环性能。(a)0.1 C下第一个循环的电压曲线,和(b)放电容量。
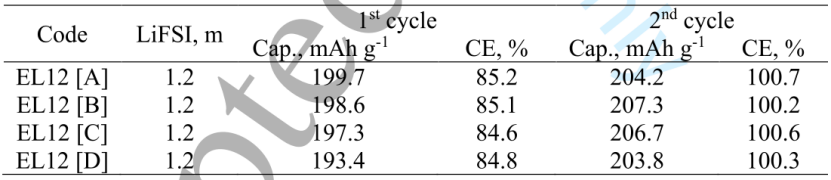
【表3】不同来源的LiFSI对Gr/NCA软包电池的比容量和库仑效率
3、总结与展望 长期以来,在锂金属和锂离子电池的中低浓度(<2.0 M)电解液中使用LiFSI作为单盐时,铝集流体的负极腐蚀一直是一个问题。不同的研究人员经常报告不一致甚至相反的结果。为了揭开LiFSI的神秘面纱,在这项工作中,使用碳酸亚乙酯和碳酸甲乙酯的3:7(wt.)溶剂体系研究了Al在0.8-1.8 m LiFSI电解质中的腐蚀行为。
这项工作导致了几个重要的发现:(1)无论LiFSI浓度如何,都存在与溶剂相关的“阈值电位”(在本系统中为4.3 V vs. Li/Li+),高于该阈值的铝会遭受无法控制的腐蚀,(2)随着LiFSI浓度的降低,轻微腐蚀偶尔会发生在~3.5 V vs. Li/Li+,但是,它可以自我修复,(3)LiFSI对SS材料具有相当的腐蚀性,因此,扣式电池制成SS材料不适合使用LiFSI电解质,(4)LiFSI可以作为单盐用于锂金属和锂离子电池的中低浓度电解质中,只要在正极处,充电电压严格限制在“阈值电位”并避免使用SS材料,并且(5)不同来源的LiFSI不会导致锂离子电池循环性能的显著差异。
考虑到成本和电池性能,1.2-1.5m的浓度范围将是锂金属和锂离子电池中使用的LiFSI电解质的最佳选择。之前关于LiFSI电解液中铝腐蚀的争议可归因于电解液溶剂对“阈值电位”的影响,如果在测试中使用扣式电池,SS垫片的腐蚀会增加额外的复杂性。
审核编辑:刘清
-
锂离子电池的类型2013-05-17 0
-
锂离子电池电解液有机溶剂的发展趋势2013-06-17 0
-
【转】锂离子电池的维护和保存技巧分享2016-08-18 0
-
锂离子电池电解液超全面介绍 有何神秘之处?2017-02-22 0
-
锂离子电池SEI膜的性能影响2019-05-24 0
-
锂离子电池简介2020-11-03 0
-
锂离子电池聚合物电解质导电机理是什么?2009-10-29 7152
-
锂离子电池及其电解质的研究2009-11-04 3349
-
锂离子电池聚合物电解质导电机理2009-12-09 2289
-
10微米厚的陶瓷电解质 让固态电池充电速度更快2020-03-24 4701
-
将商业化锂离子电池中的液态电解质替换什么解质?2020-06-09 2658
-
新型固体材料可替代电池中的易燃液体电解质2020-09-25 968
-
锂离子电池堆电解质的要求及对电池性能的影响2020-12-30 4185
-
锂离子电池电解质的基本要求2022-05-10 4845
-
讨论高压锂离子电池的老化机理及电解质设计策略2022-12-02 1561
全部0条评论

快来发表一下你的评论吧 !

